在无菌注射剂生产的复杂链条中,每一个环节都关乎药品的安全与患者的生命。从物料准备到灌封,风险无处不在。而在当前全球监管趋严的背景下,一个长期被忽视的关键风险点正在成为审计的重点与合规的痛点:已灭菌的关键组件(如胶塞)在进入A级核心区前的“一公里”无菌传递。
欧盟GMP附录1(2022修订版)明确指出:“将设备和材料传递进出洁净室和A级等关键区域,是最大的潜在污染源之一。”
法规要求,只有经过验证并列入批准清单的物料,才能通过特定的传递方式进入A/B级区。这意味着,仅完成胶塞的清洗和灭菌是远远不够的,如何在整个传递和暂存过程中维持其“无菌状态”,已成为现代污染控制策略(CCS)不可或缺的一环。这一全球性的监管聚焦,与我国2025年3月新发布的《药品生产质量管理规范》无菌药品附录(征求意见稿)所强调的方向高度一致。
法规审视:胶塞无菌性的多重挑战

随着监管深入,USP标准已从关注组件本身(<381>)发展为强调整个包装系统的功能适用性。刚刚生效的USP
<382>要求对容器密封系统(如胶塞-西林瓶组合)进行全面的功能测试与验证,这对确保无菌组件从灭菌到灌装全流程的完整与可靠,提出了更系统化的合规挑战。
微生物再污染的窗口期风险:经过蒸汽灭菌柜处理的胶塞,在从灭菌柜出口到被装入无菌传递袋、再通过传递窗进入灌装线的过程中,暴露在洁净区(如C级)环境中。任何气流扰动、人员操作或非无菌接触面都可能带来微粒和微生物的污染。
混淆与交叉污染的仓储管理风险:大批量、多批次的胶塞灭菌后,若采用敞口容器或简单覆盖的方式在洁净区暂存,极易发生批次混淆。同时,频繁的开合取用为交叉污染创造了条件,可能迫使企业面临对整批胶塞进行“二次灭菌”的艰难抉择,而这本身就是一个重大的质量缺陷。
审计追溯性的缺失风险:无论是欧盟GMP附录1还是中国GMP,都强调过程的可追溯性。传统的转移方式难以清晰记录每一袋胶塞的灭菌批次、传递时间、有效期及操作人员,在审计时面临挑战。
这些风险点,正是新版GMP及USP法规着力要求企业通过技术手段进行封闭和控制的环节。
解决方案:构建一个可验证、可追溯的无菌传递屏障
要系统性解决上述风险,必须引入一个可靠、密闭且可验证的无菌屏障系统。这并非简单的“装袋”,而是构建一个从灭菌后到使用前的全封闭无菌保护链。这正是敖卓生物所提供的专业灭菌包装解决方案的核心价值所在。
针对胶塞无菌转移的特殊场景,我们建议并提供的解决方案如下表所示,其如何精准回应法规与质量挑战:
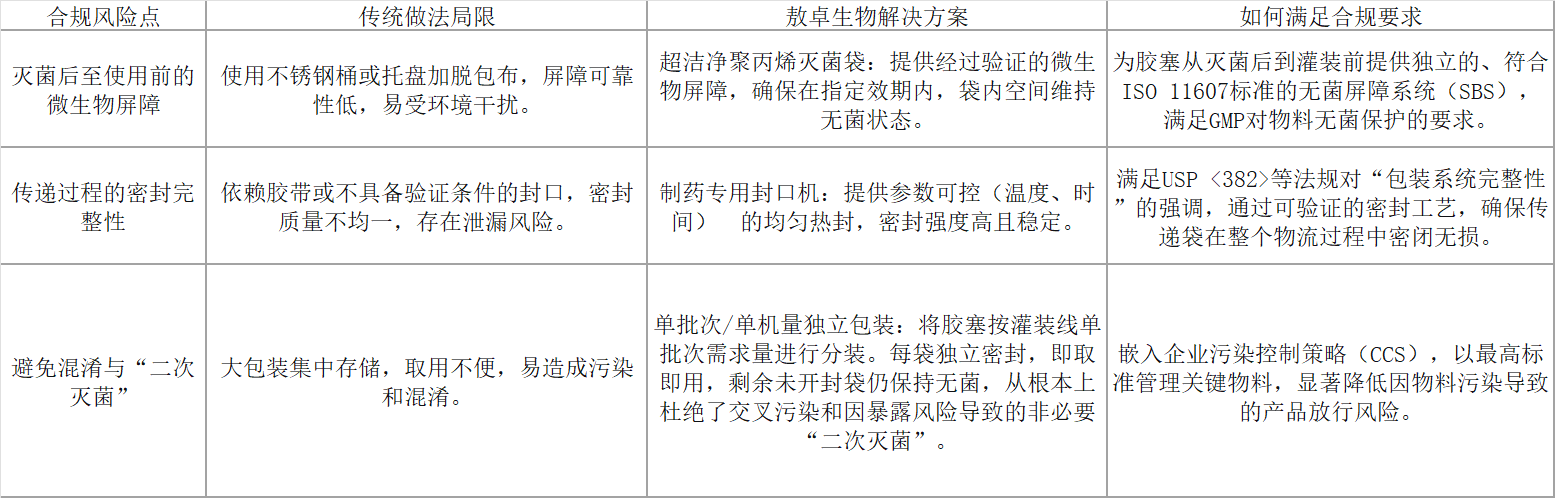
在当今的监管环境下,选择包装解决方案已不再是简单的物料采购,而是一项关乎产品质量体系稳健性的战略决策。面对胶塞、铝盖等关键无菌组件传递的合规挑战,碎片化的应对措施已显不足。
上海敖卓生物深耕制药无菌包装领域,我们不仅提供高性能的灭菌呼吸袋和精准可靠的制药专用封口机,更致力于成为您构建全方位无菌屏障系统的合作伙伴。我们从您的工艺风险出发,提供从包装材料选型、密封工艺验证到操作流程优化的全链条支持,帮助您将胶塞传递这一关键操作,从潜在的污染风险点,转变为牢固、可信、经得起审计的质量控制节点。
让我们携手,共同守护无菌生产的每一个环节,让每一枚胶塞都安全、可靠地抵达它的岗位。