前言
2026版《药品生产质量管理规范》无菌药品附录(征求意见稿)对无菌药品生产提出了更科学、更严谨的要求。敖卓生物三大核心产品(ULTRA灭菌呼吸袋、制药专用封口机、干箱手套)严格对标新附录要求,为客户提供合规、高效、可靠的无菌屏障解决方案。本解读结合附录原文条款,详细阐述敖卓产品如何精准满足法规要求。

一、灭菌包装的密封性验证要求
出处:第9章第1节第166条
内容:
"(一)应当确认密封包装能zui大限度地防止微生物、微粒和细菌内毒素/热原或化学污染,并适用于所选的灭菌方法。
(二)包装密封工艺应当经过验证。验证时应当考虑无菌保护屏障系统的完整性、灭菌前的zui长保存时限和灭菌后物品的zui长使用时限。
(三)灭菌后物品在使用前均应当检查密封包装的完整性。"
解读:
该条款明确要求密封包装必须确保无菌屏障完整性,并对密封工艺进行系统验证。
ULTRA灭菌呼吸袋:热合强度≥7N/15mm(比行业标准高近一倍),爆袋率下降90%,确保无菌保护屏障系统完整性
制药专用封口机:提供精确温控(精度±1℃)、压力(90~120N/mm²)和时间(0.2~6秒)控制,确保每次封口均一可靠
验证支持:提供完整的密封工艺验证方案模板,包括微生物挑战法(SAL≤10⁻⁶)等适用验证方法资料,协助客户完成"无菌保护屏障系统完整性"验证
二、灭菌后物品的包装保护和贮存
出处:第9章第1节第165条
内容:
"灭菌后应当提供适当的保护以防止再次污染。灭菌后不立即使用的物品,应当在密封状态下贮存,并验证zui长保存时限。使用密封包装保护灭菌物品时,应当在灭菌前完成包装操作。"
解读:
该条款强调灭菌后物品必须在验证的保存时限内保持无菌状态。
无菌保持验证:ULTRA灭菌呼吸袋提供12个月无菌保持验证报告(第三方机构出具),符合行业标准要求,支持客户验证自身工艺的"zui长保存时限"
产品有效期:未灭菌呼吸袋有效期5年,确保客户在使用前材料性能稳定可靠
材料优势:93g/m²聚丙烯多孔性材料(孔径31μm),确保灭菌后水汽完全蒸发,避免微生物滋生风险
操作合规:灭菌前完成包装操作,确保物品在灭菌过程中得到充分保护
三、灭菌指示和区分已灭菌/待灭菌物品
出处:第9章第1节第164条
内容:
"应当明确区分已灭菌物品和待灭菌物品。每一车(盘或其他装载设备)产品或物料均应当有标识(或电子追踪),清晰地注明品名、批号并标明是否已经灭菌。必要时,可用湿热灭菌指示带、辐照灭菌指示剂等加以区分。"
解读:
该条款要求建立清晰的灭菌状态标识系统,防止混淆风险。
内置灭菌指示剂:ULTRA灭菌呼吸袋采用灰色→深黑色变色指示剂(符合EN ISO 11140-1 1类工艺指示剂标准),无脱落风险,变色对比度高,肉眼识别清晰
优势:内置设计避免标签脱落风险,支持电子追踪系统集成,完全满足"明确区分已灭菌物品和待灭菌物品"的要求
合规性:颜色变化不可逆,灭菌后自动变色,减少人为错误,符合附录对标识清晰性的要求
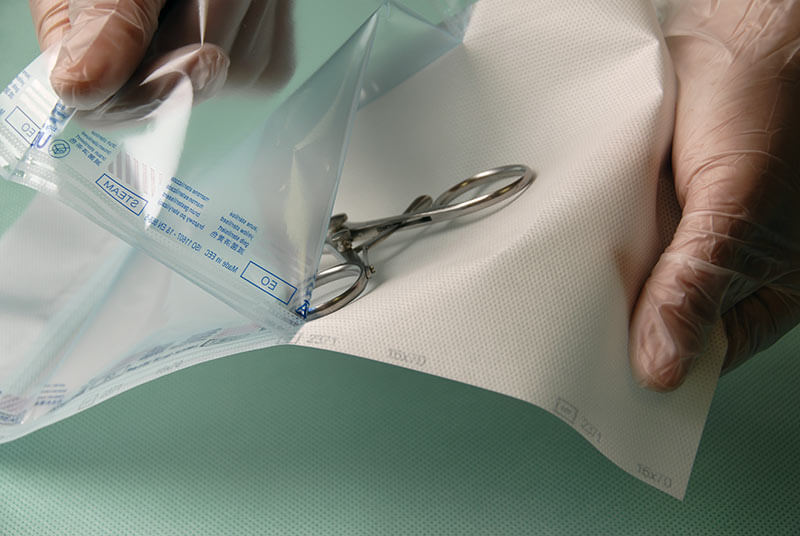
四、包装材料适用于多种灭菌方法
出处:第9章第2节第169条(六)
内容:
"除已密封的产品外,待灭菌物品应当干燥,应当用合适的材料适当包扎,所用材料及包扎方式应当有利于空气排放、蒸汽穿透并在灭菌后能防止污染。"
解读:
该条款针对湿热灭菌,要求包装材料允许蒸汽穿透同时防止污染,并隐含对多种灭菌方式的兼容性要求。
五、密封工艺的关键参数控制
出处:第10章第1节第198条
内容:
"FFS的关键工艺参数应当在设备确认期间确定,应当至少包括:......(三)密封温度、密封温度均匀性、密封时间和压力。"
解读:
该条款虽针对FFS技术,但其对密封参数控制的要求适用于所有密封工艺。
六、包装完整性的检查和验证
出处:第8章第4节第131条
内容:
"无菌药品应当使用经验证的方法进行密封,避免产品遭受污染。包装容器密封性验证应当考虑运输条件(如减压或极端温度)可能对容器密封性产生的不利影响。"
解读:
该条款强调密封性验证需考虑实际使用条件,并明确验证方法的适用性。

七、无菌物品的转移和表面消毒
出处:第9章第1节第166条(四)、(五)
内容:
"(四)灭菌后物品应当使用经验证的方法转入A级区,应当证明转移方法能够有效控制对A级和B级区的潜在污染风险。可以考虑使用快速传递接口技术。
(五)灭菌后物品转入A级区时应当对密封包装的外表面进行消毒,并证明消毒方法能将包装上的污染降低至进入A/B级区的可接受水平。"
解读:
该条款对无菌物品转移过程的污染控制提出明确要求。
转移支持:ULTRA呼吸袋外表面平滑设计,便于在转移至A/B级区时进行表面消毒,支持快速传递接口(RTP)技术
消毒兼容性:材料可兼容常用消毒剂(如75%酒精、过氧化氢等),确保消毒后包装完整性不受影响
风险控制:配合内置灭菌指示剂(灰色→深黑色),无脱落风险,便于操作人员快速识别灭菌状态,降低转移过程中的混淆风险
八、包装材料的微生物和微粒控制
出处:第3章第1节第18条
内容:
"无菌生产所用的包装材料、容器具、设备和其他任何物品均应当灭菌。应当通过双扉灭菌柜、双扉去热原烘箱、隧道烘箱,或以其他能避免引入污染的方式进入无菌生产区。"
解读:
该条款要求包装材料进入无菌生产区时不得引入污染。
初始污染物控制:ULTRA灭菌呼吸袋提供初始污染物证明材料,确保进入洁净区时不会引入污染
微粒控制:"洁净剥离"特性(无纤维撕裂风险,开启时无微粒释放、不需要剪刀裁开),符合ISO 14644-1标准对A级洁净区的要求
材料安全性:采用药用级别材料,通过可提取物和浸出物测试,确保不对药品质量产生不良影响
九、隔离器和RABS手套系统要求
出处:第2章第2节第28条
内容:
"隔离器和RABS手套系统的材料应当具有适当的机械和化学耐受性,手套更换的频率应当在CCS中说明。
(一)隔离器:应当采用经验证的方法定期对隔离器的手套系统进行完整性测试...
(二)RABS:RABS中用于A级区操作的手套应当在安装前进行灭菌,并在每个生产周期开始前采用经验证的方法进行灭菌或去除微生物污染..."
解读:
该条款对隔离操作手套的材质、耐受性和更换频率提出明确要求。
材质优势:
灭菌兼容性:耐受过氧化氢、γ射线、121℃高温蒸汽等多种灭菌方式
使用寿命:出厂质保期4年,远超同类竞品,支持客户在CCS中明确规定更换周期
合规认证:通过FDA、CE(编号CE0598)、EN388、EN ISO 374-1等认证,确保产品质量和安全性
完整性测试支持:提供手套完整性测试方法和频率建议,支持企业建立完善的CCS

十、敖卓生物产品组合优势总结
2026版无菌附录要求 | 敖卓解决方案 | 核心价值 |
密封性验证
(第166条) | 呼吸袋热合强度≥7N/15mm + 封口机精准参数控制 + 微生物挑战法验证支持 | 爆袋率下降90% 验证效率提升50% |
无菌保持期验证
(第165条) | 12个月无菌保持验证报告 + 5年产品有效期 | 符合行业标准 支持客户验证自身工艺 |
灭菌状态标识
(第164条) | 内置灭菌指示剂(灰色→深黑色) | 避免标签脱落风险 支持电子追踪 |
多灭菌方式兼容
(第169条) | 兼容湿热(121℃/134℃)、EO、VHP | 传统材料 仅兼容湿热121℃ |
密封参数控制
(第198条) | 温度精度±1℃,均匀性≤2℃ | 比行业标准(±5℃) 更精准 |
密封性验证方法
(第131条) | 微生物挑战法、染色液渗透法验证支持 | 针对多孔材料特性 提供合规方案 |
A级区转移支持
(第166条) | 外表面平滑设计,支持RTP技术 | 降低洁净区污染风险 |
微粒控制
(第18条) | "洁净剥离"开启,无纤维撕裂风险 | 符合ISO 14644-1标准 |
隔离操作安全
(第28条) | CSM/丁腈橡胶手套,质保4年 | 机械化学耐受性优异 降低更换频率 |
结语:专业、透明、可靠
2026版无菌药品附录征求意见稿对无菌屏障系统提出了更科学、更严谨的要求。敖卓生物始终秉持专业精神:
✅ 数据真实透明:明确区分"无菌保持期(12个月)"与"产品有效期(5年)"
✅ 方法科学合规:针对多孔材料特性,提供微生物挑战法等适用验证方案
✅ 细节精益求精:内置灭菌指示剂,无脱落风险
✅ 支持全面到位:提供完整的验证模板、参数指南及专业技术支持
敖卓生物——专注洁净灭菌解决方案,以专业与诚信助力客户合规生产!